#cfs #fsc #lỗisai #lưuhành #côngbố #thiếtbịytế #thựcphẩmchứcnăng #nhậpkhẩu
Đối với các doanh nghiệp xuất nhập khẩu, CFS có lẽ không còn là loại giấy tờ xa lạ. Và đối với việc xuất nhập khẩu trang thiết bị y tế, CFS là một trong những yếu tố quan trọng nhất quyết định sản phẩm có được phép lưu hành trên thị trường hay không. Tuy nhiên, rất nhiều doanh nghiệp vẫn thường mắc lỗi khi làm chứng nhận này, dẫn đến không thể xuất/ nhập khẩu các loại trang thiết bị y tế. Do đó, bài viết hôm nay em Trang xin phép tổng hợp những lỗi sai CFS mà doanh nghiệp thường gặp dẫn đến không được duyệt lưu hành hoặc vào thầu.
Anh chị cần tư vấn, check CFS, hồ sơ miễn phí và hướng dẫn chuẩn hoá hồ sơ về TBYT, LH em Thúy 0979785886 hỗ trợ nhé
A. CFS là gì?
Giấy chứng nhận Certificate of Free Sale là giấy chứng nhận do cơ quan nhà nước có thẩm quyền của nước xuất khẩu cấp cho thương nhân xuất khẩu sản phẩm, hàng hóa ghi trong CFS để chứng nhận rằng sản phẩm, hàng hóa đó được sản xuất và được phép lưu hành tự do tại nước xuất khẩu.
Giấy chứng nhận Certificate of Free Sale có tên tiếng Việt là giấy chứng nhận lưu hành tự do hay còn gọi tắt là CFS, giấy phép này thực hiện theo Quyết định 10/2010/QĐ-TTg ban hành ngày 10 tháng 02 năm 2010. Quyết định này quy định việc cấp Giấy phép lưu hành tự do (CFS) đối với sản phẩm, hàng hóa được sản xuất trong nước để xuất khẩu và việc yêu cầu Giấy phép lưu hành tự do đối với sản phẩm, hàng hóa nhập khẩu để lưu thông tại Việt Nam.
CFS cũng có thể có một số tên gọi khác nhưu CPP, FSC.
B. Cơ quan cấp CFS cho trang thiết bị y tế?
Bộ Y tế là cơ quan có thẩm quyền cấp CFS cho TBYT, cụ thể, Bộ có thẩm quyền cấp CFS đối với:
– Thực phẩm chức năng, thực phẩm tăng cường vi chất dinh dưỡng, thực phẩm bổ sung, phụ gia thực phẩm, nước uống, nước sinh hoạt, nước khoáng thiên nhiên; thuốc lá điếu; hóa chất, chế phẩm diệt côn trùng, diệt khuẩn dùng trong lĩnh vực gia dụng và y tế
– Thuốc, mỹ phẩm
– Trang thiết bị y tế.
Đối với CFS cho hàng nhập khẩu, ngoài CFS do BYT nước xuất khẩu, cần phải xin hợp pháp hoá lãnh sự để được chấp thuận lưu hành tại Việt Nam. Anh chị tham khảo quy trình xin cấp CFS nước xuất khẩu như sau:
C. Các bước để hợp pháp hóa lãnh sự CFS
Trước tiên, sau khi văn bản đã có chữ ký và con dấu của người đại diện của cơ quan có thẩm quyền cấp CFS, cơ quan có thẩm quyền của nước sở tại (có thể là Bộ ngoại giao của nước sở tại) sẽ xác thực chữ ký và con dấu của người đứng đầu cơ quan này.
Sau đó văn bản sẽ tiếp tục được cơ quan có thẩm quyền của Việt Nam đặt tại nước sở tại hợp pháp hóa (có thể Đại sứ quán hoặc Tổng Lãnh sự quán của Việt Nam). Sau khi đã hợp pháp hóa đầy đủ các bạn có thể gửi về Việt Nam để sử dụng.
Đối với một số nước cơ quan đại diện của nước đó tại Việt Nam có thẩm quyền Hợp pháp hóa các bạn hoàn toàn có thể gửi về Việt Nam để Hợp pháp hóa, khi đó các cơ quan có thẩm quyền sẽ là:
- Đại sứ quán/ Tổng lãnh sứ quán của nước ban hành văn bản tại Việt Nam;
- Cục Lãnh sự – Bộ Ngoại giao Việt Nam/ Sở Ngoại vụ TP Hồ Chí Minh.
D. Các lỗi sai thường gặp trong CFS?
- Sai tên hàng, thiếu tên Model.
Đây là một lỗi rất cơ bản trên CFS, đã được quy định tại Mục 3, khoản 3 Điều
10 của NĐ 69/2018/NĐ-CP hướng dẫn luật quản lý ngoại thương:
“CFS phải có thông tin tối thiểu sau :
…e) Trên CFS phải ghi rõ là sản phẩm , hàng hóa được sản xuất và được
phép bán tự do tại thị trường của nước sản xuất hoặc nước cấp CFS”
– CFS chỉ đc phép xuất khẩu chứ ko dc lưu hành tại nc sở tại ( CFS Hàn rất hay mắc phải lỗi này). Chuẩn sẽ phải là : ” Freely sold in domestic and overseas markets”
👉👉👉 Vì vậy nếu CFS thiếuthông tin này thì bộ hồ công bố hoặc lưu hành sẽ không được chấp nhận
- CFS thiếu con dấu/ sai con dấu của đơn vị cấp phép/ Sai cơ quan cấp phép:
- Có hai loại con dấu trên CFS Trung Quốc được Bộ y tế Việt Nam chấp thuận:
Dấu của Cơ quan Quản lý Dược các tỉnh ( Liên hệ ngay em THÚY 0979785886 để biết thêm chi tiết ) - Dấu của Cục Quản lý sản phẩm Y tế Quốc gia cấp Trung ương ( National Medical Products Administration – NMPA) – Trung Quốc (theo Nghị định 98)
- OMETA của Nhật hiện chưa đc chấp nhận hay cơ quan TQ ( China Chamber of Commerce for Import and Export of Medicines & Health Products)
- CFS thiếu hợp thức hóa lãnh sự
Khi CFS đã được cấp phép nhưng thiếu hợp thức hóa lãnh sự của đại sứ
quán Việt Nam tại Trung Quốc, thì CFS này cũng được coi là không hợp lệ,
phải bổ sung hợp thức hóa lãnh sự.
- CFS hết hạn sử dụng
- CFS không thể hiện mối quan hệ giữa nhà sản xuất và nhà nhập khẩu:
– CFS chỉ có tên, địa chỉ của nhà sản xuất chứ ko cấp cho chủ sở hữu trang thiết bị y tế dù nhà máy và CSH khác nhau => CFS này cũng không được chấp nhận
– Việc CFS chỉ có tên của Chủ sở hữu Trang TBYT, ko có tên của nhà sản xuất ( thường với các Đơn vị gia công OEM) thì lúc này sẽ phải làm giải trình mối quan hệ và hợp thức hóa thư giải trìn

CFS này không được chấp nhận bởi nó được soạn thảo cho bên quan tâm để đệ trình lên Cơ quan Y tế của AI CẬP nên nếu dùng làm hồ sơ vào thầu và lưu hành ở Việt Nam được, bên cạnh đó thì CFS này cũng chưa được hợp pháp hoá lãnh sự, vì vậy là không hợp lệ.
E. CFS CÁC NƯỚC THAM CHIẾU ĐỂ VÀO THẦU:
Mục đích cần có CFS tham chiếu là để hồ sơ lưu hành được đưa vào luồng cấp nhanh, cũng như tăng hạng thầu cho doanh nghiệp. Bên em đã làm đc CFS Úc, Anh để nâng hạng thầu, bác nào cần alo em THÚY nhé 0979785886
DANH SÁCH CÁC NƯỚC THAM CHIẾU:
1. Các nước khu vực Châu Âu:
- Cộng hòa Áo;
- Cộng hòa Romania;
- Cộng hòa Ba Lan
- Cộng hòa Séc;
- Cộng hòa Bồ Đào Nha
- Cộng hòa Síp;
- Cộng hòa Bulgaria
- Cộng hòa Slovakia;
- Cộng hòa Croatia
- Cộng hòa Slovenia;
- Cộng hòa Estonia
- Cộng hòa Tây Ban Nha;
- Cộng hòa Hungary
- Cộng hòa Ý;
- Cộng hòa Hy Lạp
- Đại công quốc Luxembourg;
- Cộng hòa Ireland
- Liên bang Thụy Sỹ;
- Cộng hòa Latvia
- Vương quốc Anh;
- Cộng hòa liên bang Đức
- Vương quốc Bỉ;
- Cộng hòa Litva
- Vương quốc Đan Mạch;
- Cộng hòa Malta
- Vương quốc Hà Lan;
- Cộng hòa Phần Lan
- Vương quốc Thụy Điển.
2. Cộng hòa Pháp;
3. Hơp̣ chủng quốc Hoa Kỳ
4. Nhật Bản.
5. Thịnh vượng chung Úc.
6. Ca-na-da.
Theo thông tư Số: 14/2020/TT-BYT của Bộ Y Tế quy định về phân nhóm và việc dự thầu của các nhóm trang thiết bị y tế như sau:
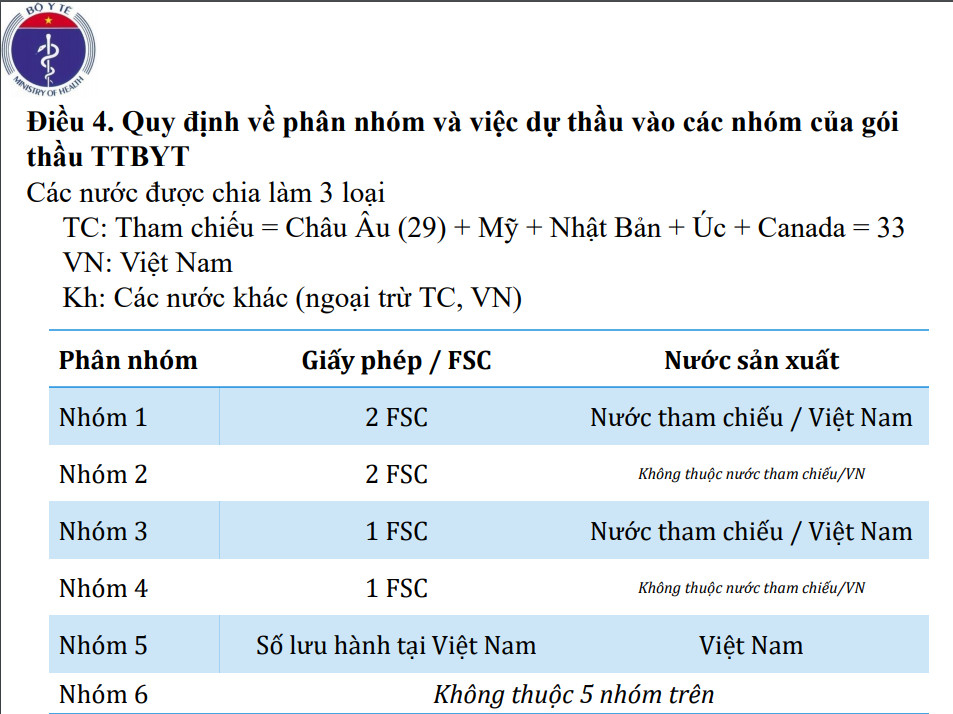
E. Một số mẫu CFS của BYT
Trên đây là tổng hợp những điểm cần lưu ý về CFS- loại giấy tờ vô cùng quan trọng và quyết định hồ sơ lưu hành có được duyệt hay không.
Chi tiết cần tư vấn thêm, anh chị liên hệ 0979785886 – MS THÚY tư vấn 24/7 nhé!
Hotline: 0979785886 (zalo/tel) – Ms THÚY – Sales Manager
Mail: thuynt@airseaglobalgroup.com.vn
Add: P2414; 2412 Tòa
Eurowindown, 27 Trần Duy Hưng, Cầu Giấy, Tp. Hà Nội, Việt Nam
AIRSEAGLOBAL GROUP
VUA DỊCH VỤ NHẬP KHẨU THIẾT BỊ Y TẾ
Đảm bảo – Uy tín – Nhanh chóng
CÁC DỊCH VỤ CUNG CẤP:
1. Xin giấy phép nhập khẩu theo thông tư 30
2. Xin đăng ký lưu hành thiết bị y tế loại BCD
3. Phân loại chỉ từ 400k ( Chuẩn vào thầu)
4. Xin Công bố đủ điều kiện kinh doanh thiết bị y tế loại BCD
5. Xin công bố tiêu chuẩn áp dụng cho thiết bị y tế loại A
6. Xin công bố đủ điều kiện sản xuất
7. Vận chuyển EXW, FOB khai hải quan trọn gói
8. Thủ tục tạm xuất tái nhập, tạm nhập tái xuất hàng y tế
9. Dịch vụ làm chứng chỉ lưu hành tự do cho hàng loại A sản xuất
trong nước.
10. Dịch vụ làm ISO 9001, ISO 13485, tất cả hồ sơ, test kiểm nghiệm
cho hàng khẩu trang y tế, khẩu trang thường, lưu hành tự do CFS, CE, FDA
11. Công bố mỹ phẩm, Thực phẩm chức năng

