Chắc rằng có nhiều anh chị nhập mặt hàng này đang băn khoăn không biết theo quy định mới cần làm những giấy tờ pháp lý gì để có thể nhập khẩu, lưu hành các loại trang thiết bị y tế. Bài viết này chia sẻ cơ bản cho các anh chị dễ hiểu nhé, từ Ms Thanh Trang Airseaglobal- đơn vị với 11 năm kinh nghiệm làm giấy phép và logistics hàng thiết bị y tế.
TBYT được chia làm 4 loại (mức độ rủi ro từ thấp đến cao): A-B-C-D
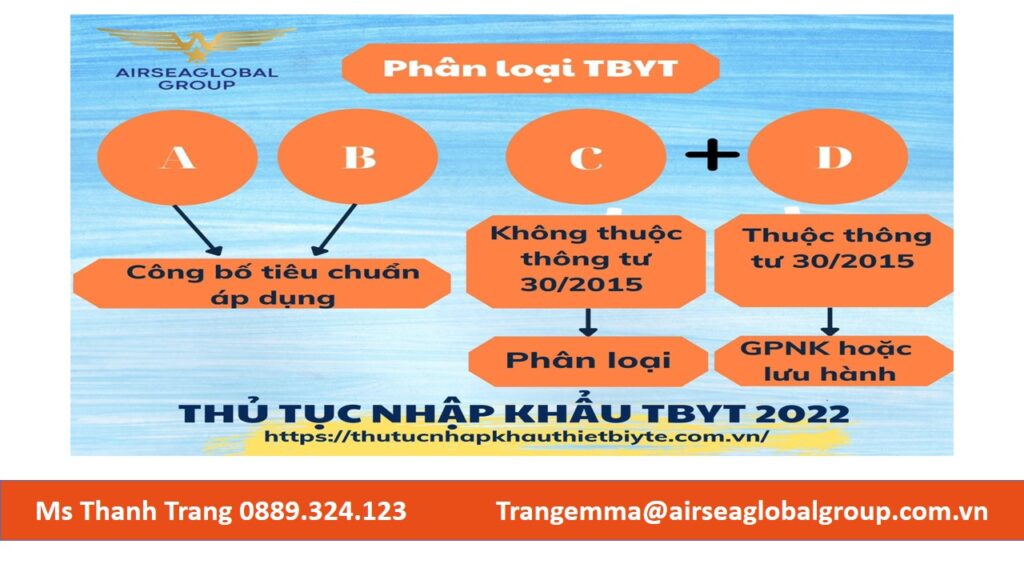
A. LOẠI A, B: Làm Công bố ở Sở y tế
Thời gian 3-10 ngày làm việc tùy Sở
Hồ sơ gồm:
- Văn bản công bố
- CFS (hợp pháp hóa lãnh sự)
- ISO 13485
- Ủy quyền (hợp pháp hóa lãnh sự)
- Bảo hành (hợp pháp hóa lãnh sự) trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế.
- Mô tả kỹ thuật
- HDSD
- Mẫu nhãn
- Bản tiêu chuẩn mà chủ sở hữu trang thiết bị y tế công bố áp dụng hoặc Giấy chứng nhận hợp chuẩn

B. LOẠI C, D
Trong 2022, nếu hàng không thuộc thông tư 30/2015 thì chỉ cần phân loại là nhập về được. Nếu hàng thuộc thông tư 30/2015 thì các bác phải có GPNK hoặc đăng ký lưu hành.
Hiện thời gian xin Đăng ký lưu hành lâu: 6-12 tháng hoặc hơn nhé
Đăng ký lưu hành sẽ xin ở Vụ TTB của Bộ Y tế
Hồ sơ đăng ký lưu hành TBYT loại C, D
Hồ sơ đề nghị cấp mới số lưu hành đối với trang thiết bị y tế khác (có cả các loại TBYT theo quy chuẩn kỹ thuật quốc gia nhưng ít nên em gửi các bác hồ sơ loại hay gặp nhất)
- Văn bản đề nghị cấp mới số lưu hành.
- CFS (hợp pháp hoá lãnh sự) đối với hàng NK hoặc công bố SX đối với hàng SX
- ISO 13485
- Uỷ quyền của chủ sở hữu trang thiết bị y tế cho cơ sở thực hiện việc đăng ký lưu hành (Hợp pháp hóa)
- Giấy xác nhận đủ điều kiện bảo hành do chủ sở hữu trang thiết bị y tế cấp, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế (hợp pháp hóa)
- Kết quả thẩm định hồ sơ CSDT của đơn vị do Bộ trưởng Bộ Y tế chỉ định kèm theo hồ sơ CSDT. ( áp dụng từ 2023)
- Đối với trang thiết bị y tế chẩn đoán in vitro là thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát phải có thêm giấy chứng nhận chất lượng do cơ quan có thẩm quyền của Việt Nam cấp.
- Hồ sơ kỹ thuật chung về trang thiết bị y tế theo quy định của ASEAN (sau đây viết tắt là hồ sơ CSDT) sẽ áp dụng từ 01.01.2023.
8.1. Tài liệu hướng dẫn sử dụng của trang thiết bị y tế
8.2. Mẫu nhãn sẽ sử dụng khi lưu hành tại Việt Nam của trang thiết bị y tế.
Các bác nào vướng mắc về giấy phép, công bố hoặc lưu hành TBYT có thể liên hệ:
Ms Thanh Trang (Emma) 0889. 324.123 (zalo)
trangemma@airseaglobalgroup.com.vn
AIRSEAGLOBAL GROUP – SỐ 1 DỊCH VỤ NHẬP KHẨU THIẾT BỊ Y TẾ TẠI VIỆT NAM
Các dịch vụ cung cấp :
– NHẬN KÊ KHAI GIÁ, CÔNG KHAI GIÁ THIẾT BỊ Y TẾ
– PHÂN LOẠI TBYT ( CÓ CHỨNG CHỈ HÀNH NGHỀ )
– LƯU HÀNH C,D (Mới nhất theo NĐ 98)
– CÔNG BỐ LOẠI A, B, CÔNG BỐ SẢN XUẤT.
– ISO9001, ISO13485, ISO22001, HACCP, ISO45001,…
– CÔNG BỐ ĐỦ ĐIỀU KIỆN KINH DOANH TBYT BCD
– HẢI QUAN THIẾT BỊ Y TẾ
– VẬN CHUYỂN AIR / SEA EXW , FOB VỀ VIỆT NAM
Mob/zalo: 0889324123- Ms Thanh Trang
Mail: trangemma@airseaglobalgroup.com.vn
Add: AIRSEAGLOBAL – Phòng 2410-2412-2414, tòa Eurowindow, 27 Trần Duy Hưng, Cầu Giấy, HN

